伴随着医美产业的发展,医疗器械产品逐渐被市场所接受认可,发展至今日已有多种不同形态的产品上市,并逐渐形成稳定的产品类型。例如,在医美项目中,以注射类为代表的非手术医美项目因其低侵入性和恢复快的特点被消费者更广泛地接受。
例如:透明质酸(玻尿酸)、胶原蛋白、肉毒素、外泌体等为原料的医美注射类产品具有塑形强、效果直观等优势,受到市场青睐。本期内容就以透明质酸(玻尿酸)填充剂为例,介绍医疗器械注射类产品的要求、注册流程以及其他注意事项。
透明质酸类注射产品概述
目前透明质酸主要通过动物组织提取法或微生物发酵法制备,根据用途和技术要求可以分为三类:医用级、化妆品级、食品级,并逐渐拓宽应用领域。其中作为注射类使用的透明质酸产品属于医用级,并列入III类医疗器械,严格监管。
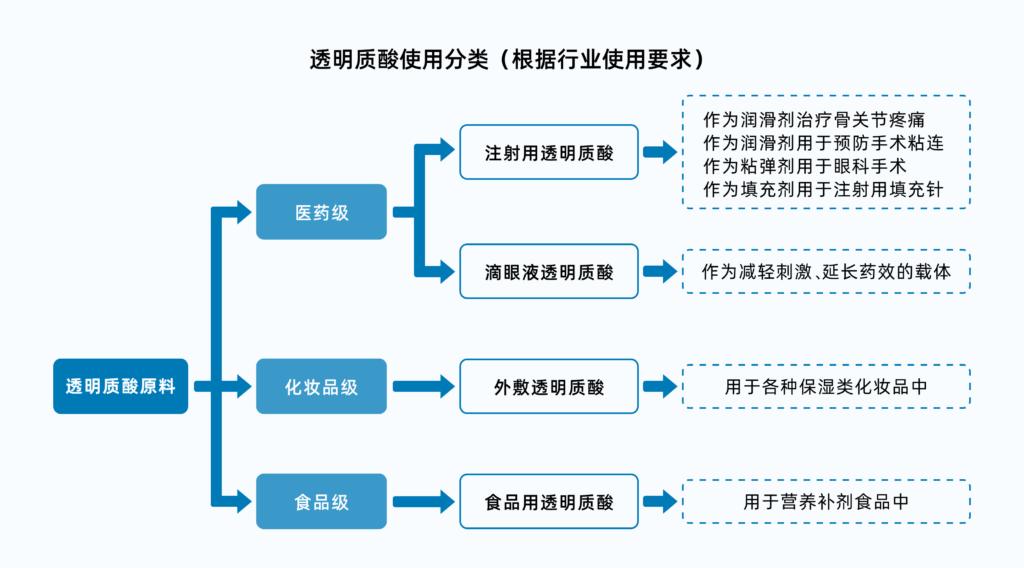
注射填充用透明质酸产品,通常由注射器以及预装在注射器中的交联透明质酸凝胶组成,用于注射到真皮层和/或皮下组织,起到填充增加组织容积的作用。为了减轻消费者注射痛感,一些透明质酸填充产品还添加了局部麻醉药物,例如盐酸利多卡因等成分。
因此,依据中国国家药品监督管理局对医用透明质酸钠类产品的分类管理规定,这类含有药物成分的透明质酸注射填充产品被界定为医疗器械属性的药械组合产品,须遵循医疗器械法规要求。
由于透明质酸易溶、吸收好、组织中停留时间较短等特性,需要经过交联改性方式处理才可用于不同细分领域。交联是指通过交联剂使透明质酸分子间发生交联,形成更具有塑性支撑能力的分子网状结构,并能增加一定的降解吸收时间。常用的交联剂有:ADH(乙二酸二酰肼),EDC(碳二亚胺),BDDE(丁二醇缩水甘油醚)等。
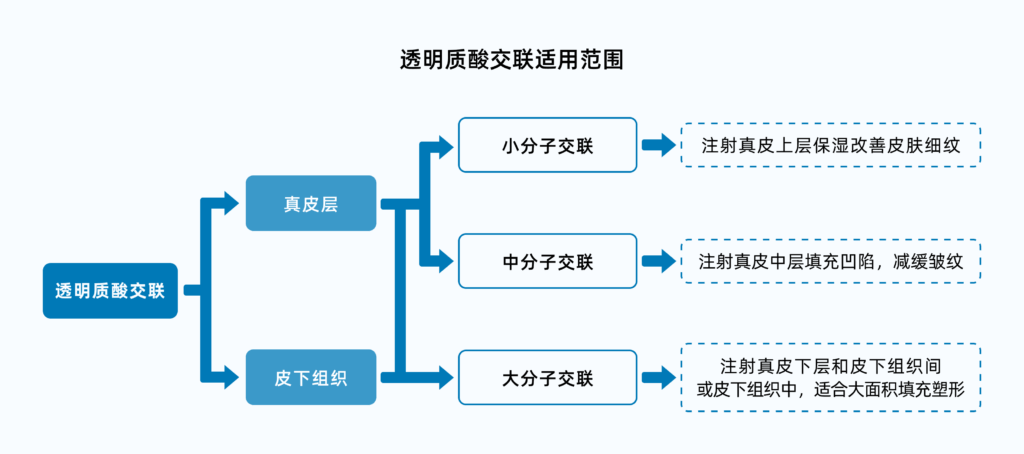
透明质酸的交联度越高,其硬度和强度就越大,更容易塑形,而交联度越低,则流动性更好,适合浅层皮肤保湿、填充等项目。
水光针:特定剂型特性介绍
近年来市场大火的水光针主要成分常为非交联或小分子交联透明质酸,借助器具将成分注入真皮层中,透明质酸的主要为保湿等作用,用于改善皮肤状态。水光针中可能还包含盐酸利多卡因等麻醉剂成分,因此水光针的性质主要为医疗器械的药械组合产品。
市场上现有的水光针主要以注射、滚针、微针、脉冲等形式,主要作用于人体皮肤真皮层或表皮层中,形式多样,多总结为以下几个类型:

注射类医疗器械产品分类体系
医疗器械注射类产品主要包括:透明质酸(玻尿酸)类、胶原蛋白类、以聚乳酸为代表的再生制剂类、肉毒素类以及新兴的外泌体类等,其中透明质酸(玻尿酸)和胶原蛋白均为医疗器械领域常用的注射类材料,通常预装载于注射器或安瓿瓶中。
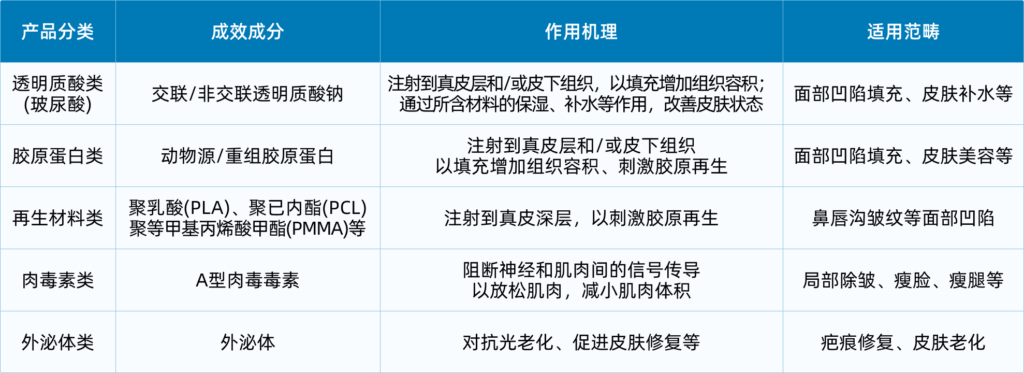
而肉毒毒素虽然广泛用于医美领域,但其属于医疗用毒性药品的范畴。
注射类医疗器械行业监管体系
医疗器械行业及所涉及的部分医美领域受到国家药品监督管理局、国家卫生健康委员会以及国家市场监督管理总局等多部门的监管。
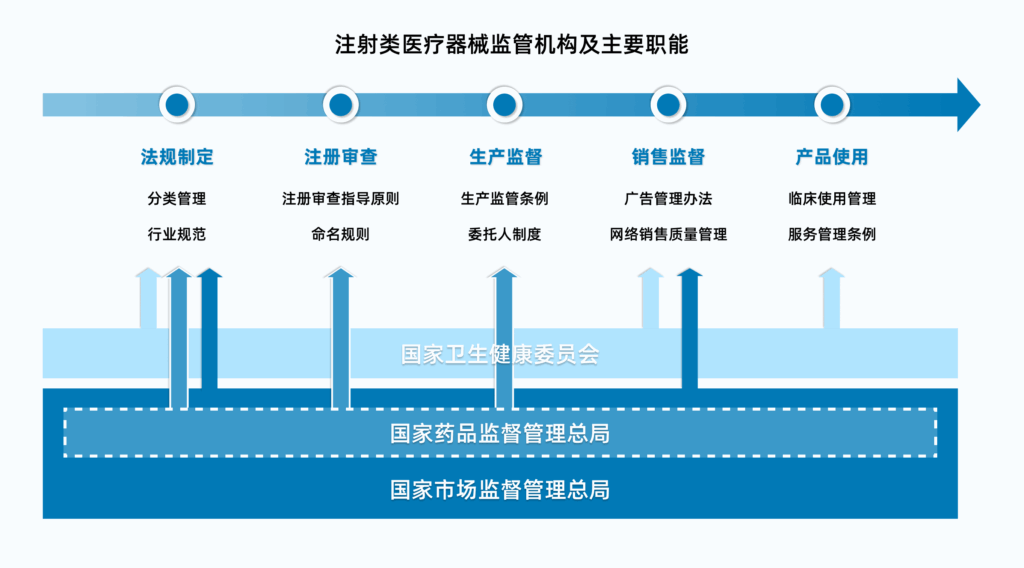
在医疗美容行业中,上述提到的透明质酸(玻尿酸)类、胶原蛋白类、再生制剂类注射产品都属于医疗器械的范畴,按照《医疗器械分类目录》进行分类管理,并受《医疗器械监督管理条例》等法规等约束。
而另一类注射产品——肉毒素类,因具有生物毒性,所以须按照《医疗用毒性药品管理办法》等相关法律法规,对肉毒素实施全链路监管。
Tips:注射用A型肉毒毒素属于医疗毒性药品,具有阻抑神经系统的作用,使用不当会引起呼吸衰竭等症状,因此,相比于其他注射类产品,生产、销售和使用都受到更加严格的管理。
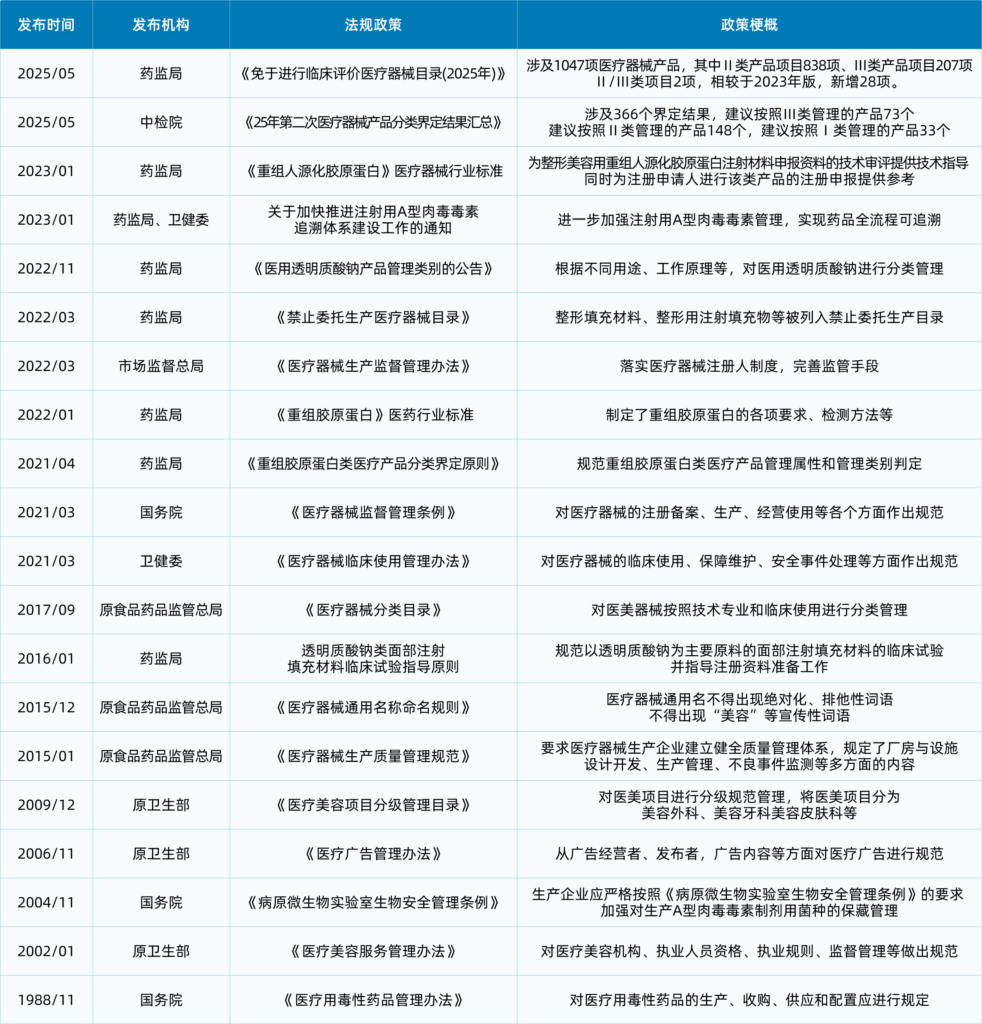
注射类医疗器械相关政策更新动态
从《医疗用毒性药品管理办法》的颁布到《医疗器械监督管理条例》的实施,注射类医疗器械的监管愈发完善,相关法规动态如下:
透明质酸注射填充剂注册要点解析
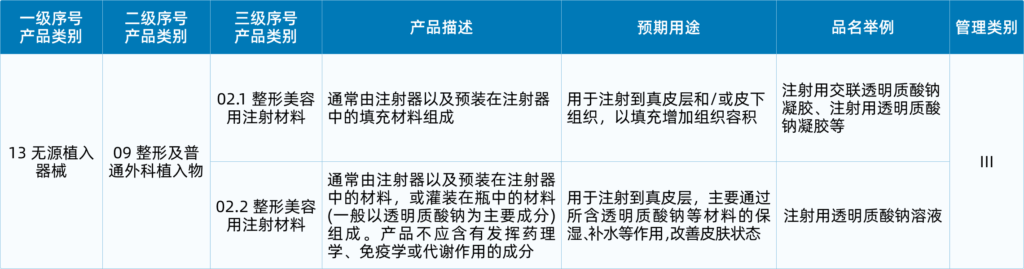
根据《整形美容用透明质酸钠类注射填充剂注册审查指导原则(2024年修订版)》(征求意见稿)我们可知,该类产品在在《医疗器械分类目录》中被定义为三类医疗器械,分类编码为13-09-02。
- 注册单元划分
首先申报应符合《医疗器械注册单元划分指导原则》的要求,考虑产品技术原理、结构组成、性能指标等因素。结合上文中提到的几种划分标准要求进行区分。
可以分为以下几种不同注册单元的情况:
(1) 不同的化学成分;
(2) 不同的浓度;
(3) 不同交联方式、交联程度;
(4) 不同的凝胶颗粒尺寸及其分布;
(5) 不同的透明质酸钠制备方式:鸡冠提取/微生物发酵。
可考虑划分为同一注册单元的情况举例:
(1) 不同装量;
(2) 不同包装,如不同类型的注射器;
(3) 搭配不同的注射针类型及数量;
(4) 相同的型号规格适用多种适用范围/适应症。
- 综述资料
详细描述产品的立题依据、研发目的、临床使用必要性等内容,并根据产品开展的研究进行概述。
产品命名依据需参照《医疗器械通用名称命名规则》《无源植入器械通用名称命名指导原则》等文件要求确定产品核心用词,如“注射填充剂”等,除此之外,还需规范产品特征词,如“交联透明质酸钠”、“含盐酸利多卡因”等。
产品作用原理需表明预期与人体接触部位(解剖部位)、接触方式、作用时间、配用器械信息(名称、注册证号及型号规格)、注射剂量及注射频率。
产品原材料介绍需表明(包括交联剂以及生产过程中成分)的中文化学名称、化学结构式/分子式、材料商品名(若有)、材料代号/牌号(若有)、在产品中发挥的功能和作用。
(1) 若原材料外购(包括交联剂以及生产过程中成分),需明确原材料供应商,提交质量控制标准、检验报告和证明文件(如药品包装材料登记备案证明或医疗器械注册证书等)。
(2) 若原材料为自行合成,需阐述生产质量控制标准并提交检测报告。透明质酸钠原料建议符合YY/T 1571的规定。若注射针、注射器无注册证书或登记备案证明,还需提交各部件组成材料的安全性支持性资料。提供注射用水的质量标准和验证报告,宜符合现行的《中华人民共和国药典》。
产品性能结构及组成需明确以下几种内容:
(1) 列出预期与人体接触的产品组分和材料;
(2) 列出终产品中所有成分及交联剂的化学名称(聚合物和交联剂需列出化学结构式)及其含量(注意颗粒和溶液需分别列出);
(3) 明确注射针规格、数量、组成材料(牌号),并给出针头局部细节图示,提供产品结构图示等;
(4) 对于化学交联的透明质酸钠,需要详细描述交联原理
如有申报产品境外上市历史,企业可提供产品境外上市情况信息,针对所申报适用范围概述产品的境外批准情况。提供不良事件和召回情况等。
- 产品性能研究
说明产品技术要求中性能指标及检验方法的确定依据,提供采用的原因及理论基础。依据产品性能研究结果、相关国家标准/行业标准,结合临床需求制定性能指标接受标准。对于自建方法,宜提供相应的依据和/或方法学验证资料。
验证资料至少包括:
(1)研究汇总列表,包括研究项目、接受标准、试验方法简述、参考技术文件、测试型号规格、测试样品批号、样品数量等。
(2) 研究项目的标准及依据
(3) 研究项目的具体试验方法
(4) 明确研究型号的选择及依据,确定不同研究项目的型号选择及数量
(5) 研究结果及分析,以及研究结论,如为定量指标,采用数据表示结果,如无法得出测试值,应明确检测方法限制。
